Plt Bupati Asmar Terima Penghargaan Cakaplah Awards 2024
Bengkalis Dinobatkan Daerah Informatif, Industri Pers Dipandang Sebelah Mata
Polsek Rangsang Ungkap Sindikat 3 Pengedar Narkoba Dalam Satu Hari
OpsTertib Ramdhan LK 2024 Sinergitas Subuh Keliling TNI POLRI
BPOM: Belum Ada Izin Edar Vaksin Covid-19
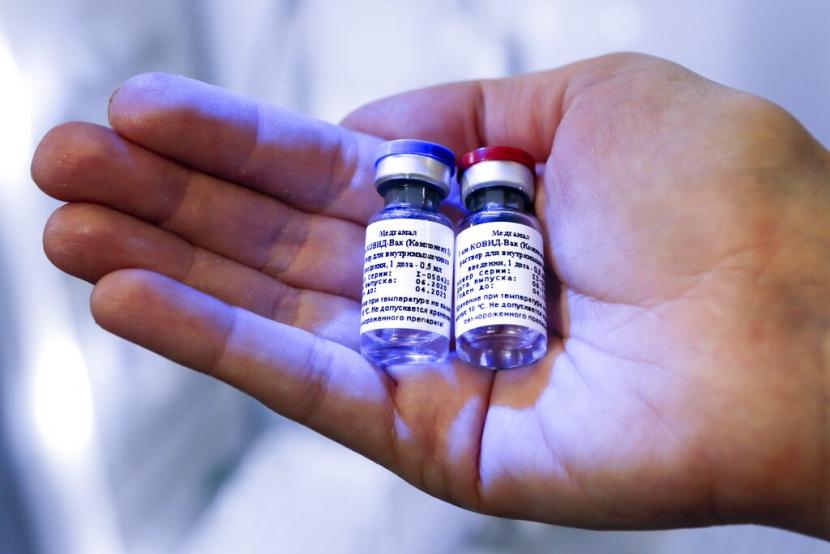
RADARPEKANBARU.COM – Badan Pengawas Obat dan Makanan (BPOM) memastikan tidak akan mengeluarkan izin penggunaan darurat (emergency use authorization) bila vaksin Covid-19 tidak aman. Aspek keamanan menjadi akan pertimbangan utama dalam memberikan persetujuan sebelum vaksin disuntikkan ke masyarakat.
Pelaksana Tugas Deputi I BPOM Togi Hutadjulu mengatakan, izin penggunaan obat dan vaksin yang dikeluarkan BPOM harus memenuhi syarat keamanan, khasiat, dan mutu yang dibuktikan melalui uji klinis yang baik. Semua itu harus mengacu pada persyaratan dan standar yang berlaku secara nasional dan internasional.
“Hingga saat ini, belum ada vaksin Covid-19 yang sudah mendapatkan izin edar. Semua kandidat vaksin yang ada masih dalam proses pengembangan diuji, baik preklinis maupun uji klinis itu sendiri,” kata Pelaksana Tugas Deputi I BPOM Togi Hutadjulu di Jakarta, Kamis (29/10).
Menurut Togi, pengambilan keputusan pemberian izin penggunaan darurat ini harus dilakukan dengan pertimbangan kemanfaatan yang lebih tinggi dari risikonya. Keputusan diambil berdasarkan hasil evaluasi data keamanan dan khasiat kandidat vaksin itu sendiri. Artinya, keamanan ada di urutan pertama.
Togi mengungkapkan, proses evaluasi keamanan dan khasiat kandidat vaksin melibatkan Tim Komite Nasional Penilai Obat yang terdiri atas ahli farmakologi, klinisi, dan pakar bidang terkait lain. Jika hasil evaluasi vaksin dinyatakan memenuhi syarat keamanan, khasiat, dan mutu, BPOM dapat memberikan persetujuan penggunaan izin darurat atau nomor izin edar (NIE).
Ketua Tim Peneliti Uji Klinis Vaksin Covid-19 dari Fakultas Kedokteran Universitas Padjadjaran (Unpad) Prof Kusnandi Rusmil mengatakan, vaksin Covid-19 buatan Sinovac, Cina, yang sedang diuji klinis tahap III di Bandung, Jawa Barat, sudah berkali-kali dicek aspek keamanannya. Jika lulus uji klinis fase III, vaksin ini bisa digunakan masyarakat secara luas.
Kusnandi menuturkan, dalam uji klinis vaksin, ada beberapa tahap seperti preklinik dan uji klinik. Dalam preklinik calon vaksin telah diuji secara fisika dan kimia pada tumbuh-tumbuhan dengan sangat ketat kemudian dilanjutkan uji pada tikus dan monyet dengan pemberian berbagai cara dan dosis. Bila aman, dilanjutkan uji klinis pada manusia. “Pada manusia ada empat tahap untuk melihat keamanan, imunogenisitas dan efikasinya,” kata dia.
Manajer Integrasi Proyek Riset dan Pengembangan Bio Farma Neni Nurainy mengatakan, Bio Farma terus melakukan pemantauan terhadap efek samping atau kejadian ikutan pascapemberian vaksin Covid-19. Dia menyebut, tidak ada satu obat pun yang sempurna sehingga pasti ada efek samping.
Dia mengatakan, apa pun kejadian ikutannya setelah vaksinasi, ada formulir yang harus diisi para relawan vaksin. Data tersebut dikumpulkan dan dianalisis. Setelah 48 jam setelah vaksinasi akan dilihat reaksi lokal dan sistemnya kemudian selama enam bulan tetap akan terus dipantau.
Neni menambahkan, berdasarkan penelitian terhadap fase I, fase II, dan beberapa laporan dari fase III, didapati bahwa gejala umum yang muncul adalah rasa sakit di tempat injeksi. Selain itu, ada juga yang merasakan gejala demam dan pusing namun sangat sedikit.
15 juta dosis
Bio Farma akan menerima 15 juta dosis bulk vaksin Covid-19 dari perusahaan biofarmasi Sinovac Biotech di Cina pada November 2020. Kepala Divisi Unit Klinik dan Imunisasi Bio Farma Mahsun Muhammadi mengatakan, dosis bulk tersebut tersebut merupakan bahan baku yang akan diolah Bio Farma di Indonesia menjadi vaksin siap guna untuk dapat didistribusikan dan diberikan kepada masyarakat.
Izin penggunaan vaksin Sinovac tersebut harus mendapatkan persetujuan dari BPOM sebelum disuntikkan ke masyarakat. Saat ini, Bio Farma telah meningkatkan kapasitas produksi untuk vaksin Covid-19 sebesar 250 juta dosis per tahun. Sementara untuk vaksin Covid-19 produk jadi dari Sinovac akan dikirim sebanyak masing-masing 1,5 juta dosis untuk November dan Desember 2020 ke Indonesia.
“Harga vaksin harus terjangkau, sudah masuk uji klinis fase III, sesuai untuk penduduk Indonesia, dan dengan biaya distribusi rendah,” ujar Mahsun.
Uji klinis fase III untuk vaksin yang dikembangkan Sinovac itu diadakan di sejumlah negara, yakni Brasil dengan 8.870 relawan penerima vaksin, Indonesia 1.620 orang, Chile 4.000 orang, Turki 13 ribu orang, dan Bangladesh 4.000 orang. Sehingga total rencana ada 31.490 orang yang menjadi sasaran vaksin tersebut.
Di sisi lain, pemerintah menegaskan akan menjamin keamanan vaksin sebelum diberikan ke masyarakat. “Jadi, saat ini kandidat-kandidat vaksin sedang dalam uji klinis fase III untuk memastikan keamanan, efek samping, dan juga rentang dosis aman yang dapat digunakan kepada manusia sehingga efektif,” ujar Juru Bicara Pemerintah untuk Penanganan Covid-19 Wiku Adisasmito.
Hingga saat ini, pemerintah masih menunggu hasil dari proses uji klinis fase III serta transfer dokumen ke BPOM untuk dianalisis. Wiku mengatakan, pemerintah menekankan agar upaya pengembangan vaksin dapat dilakukan secara hati-hati dan tidak terburu-buru, serta berpedoman pada standar kesehatan.(rep)
Sah, Prabowo-Gibran Presiden dan Wapres Terpilih
RADARPEKANBARU.COM - Komisi Pemilihan Umum (KPU) resmi menetapkan pasangan Prabowo Subianto dan Gibr.
Hari Ini Program Makan Siang dan Susu Gratis Dibahas KPK
RADARPEKANBARU.COM - Putusan Mahkamah Konstitusi (MK) terkait Perselisihan Hasil Pemilihan Umum (PHP.
Sejarah Tercipta, Bantai Yordania, Indonesia U-23 Lolos ke Fase Gugur Piala Asia 2024
RADARPEKANBARU.COM - Timnas Indonesia sukses melaju ke babak gugur setelah memas.
Putusan MK Diharapkan Tanpa Tekanan Pihak Manapun
RADARPEKANBARU.COM - Menjelang putusan Mahkamah Kons.
Gol Komang Teguh Buka Peluang Timnas U-23 Lolos 8 Besar
RADARPEKANBARU.COM - Tampil percaya diri, Timnas Indonesia U-23 menang atas Australia dengan skor ti.
Pakar: Pengajuan Amicus Curiae di Pengujung Sidang MK Bentuk Intervensi
RADARPEKANBAARU.COM - Pakar hukum tata negara dari Universitas Muslim Indonesia (UMI) Makassar Fahri.










